Kit di estrazione e amplificazione di colture OGM
Caratteristiche
■ Ampia applicabilità: questo kit può estrarre DNA genomico di alta qualità da cinque principali colture OGM.
■ Semplice e veloce: l'estrazione del DNA genomico delle colture OGM può essere completata entro 2 ore. Nessuna necessità di grandi centrifughe refrigerate, bassi requisiti per strumenti e attrezzature. Adatto per l'estrazione rapida del DNA genomico di colture OGM a tutti i livelli degli istituti di ricerca.
■ Elevata efficienza e specificità: l'esclusivo tampone della Taq polimerasi modificata dall'anticorpo assicura un'efficiente amplificazione della polimerasi, che è più specifica della normale Taq polimerasi.
Applicazioni
Il kit può estrarre DNA genomico di alta qualità dalle principali colture OGM come grano, mais, riso, cotone e soia ed eseguire il rilevamento PCR transgenico su colture OGM.
Tutti i prodotti possono essere personalizzati per ODM/OEM. Per dettagli,fare clic su Servizio personalizzato (ODM/OEM)
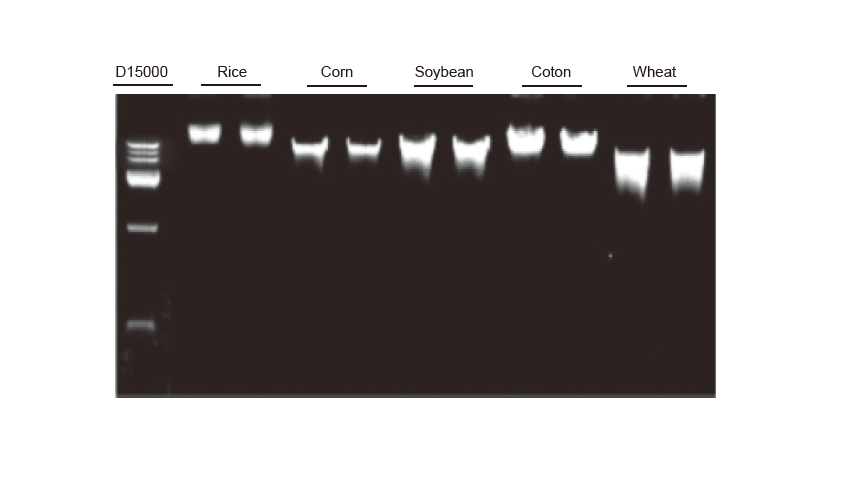 |
Estrazione del DNA genomico L'estrazione del DNA genomico è stata eseguita su foglie da 100 mg di riso, mais, soia, cotone e frumento, rispettivamente. L'esperimento è stato ripetuto due volte. Sono stati caricati 3 μl di DNA dal totale di 100 μl di eluenti per corsia. La concentrazione del gel di agarosio era del 2%. L'elettroforesi è stata eseguita sotto 6 V/cm per 20 min. D15000: Marcatore DNA TIANGEN D15000. |
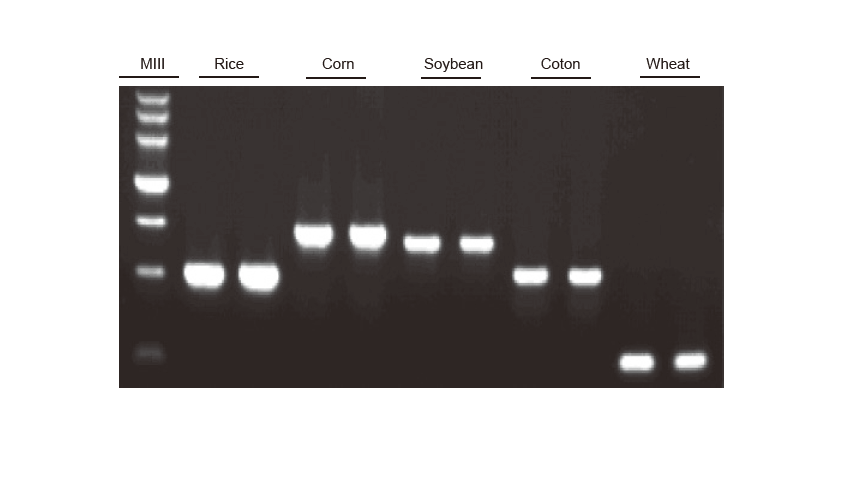 |
Rilevamento PCR Il DNA genomico di riso, mais, soia, cotone e grano è stato amplificato, rispettivamente. L'esperimento è stato ripetuto due volte. Sono stati caricati 6 μl dal sistema di reazione totale di 20 μl per corsia. La concentrazione del gel di agarosio era del 2%. L'elettroforesi è stata eseguita sotto 6 V/cm per 20 min. D15000: Marcatore DNA TIANGEN D15000. |
Modello A-1
■ Il modello contiene impurità proteiche o inibitori Taq, ecc. ——Purificare il modello di DNA, rimuovere le impurità proteiche o estrarre il DNA modello con i kit di purificazione.
■ La denaturazione del templato non è completa ——Aumentare opportunamente la temperatura di denaturazione e prolungare il tempo di denaturazione.
■ Degrado del modello ——Ripreparare il modello.
A-2 Primer
■ Scarsa qualità dei primer ——Risintetizzare il primer.
■ Degradazione del primer ——Aliquotare i primer ad alta concentrazione in un piccolo volume per la conservazione. Evitare il congelamento e lo scongelamento multiplo o la crioconservazione a lungo termine a 4°C.
■ Progettazione inadeguata dei primer (es. lunghezza del primer non sufficiente, dimero formato tra i primer, ecc.) - Riprogettazione dei primer (evitare la formazione di dimero di primer e struttura secondaria)
A-3 mg2+concentrazione
■ Mg2+ la concentrazione è troppo bassa ——Aumentare adeguatamente Mg2+ concentrazione: Ottimizza il Mg2+ concentrazione mediante una serie di reazioni da 1 mM a 3 mM con un intervallo di 0,5 mM per determinare il Mg . ottimale2+ concentrazione per ogni stampo e primer.
A-4 Temperatura di ricottura
■ L'elevata temperatura di ricottura influisce sul legame del primer e del modello. ——Ridurre la temperatura di ricottura e ottimizzare la condizione con un gradiente di 2°C.
A-5 Tempo di estensione
■ Tempo di estensione breve: aumenta il tempo di estensione.
Fenomeni: i campioni negativi mostrano anche le bande della sequenza bersaglio.
A-1 Contaminazione della PCR
■ Contaminazione incrociata della sequenza target o dei prodotti di amplificazione ——Fare attenzione a non pipettare il campione contenente la sequenza target nel campione negativo oa versarli fuori dalla provetta da centrifuga. I reagenti o l'attrezzatura devono essere sterilizzati in autoclave per eliminare gli acidi nucleici esistenti e l'esistenza di contaminazione deve essere determinata mediante esperimenti di controllo negativo.
■ Contaminazione dei reagenti ——Aliquotare i reagenti e conservarli a bassa temperatura.
A-2 Primor
■ Mg2+ la concentrazione è troppo bassa ——Aumentare adeguatamente Mg2+ concentrazione: Ottimizza il Mg2+ concentrazione mediante una serie di reazioni da 1 mM a 3 mM con un intervallo di 0,5 mM per determinare il Mg . ottimale2+ concentrazione per ogni stampo e primer.
■ Progettazione del primer non corretta e la sequenza target ha omologia con la sequenza non target. ——Riprogettazione dei primer.
Fenomeni: le bande di amplificazione della PCR non sono coerenti con le dimensioni previste, sia grandi che piccole, o talvolta si verificano sia bande di amplificazione specifiche che bande di amplificazione non specifiche.
A-1 Primer
■ Scarsa specificità del primer
——Riprogettazione del primer.
■ La concentrazione di primer è troppo alta ——Aumentare adeguatamente la temperatura di denaturazione e prolungare il tempo di denaturazione.
A-2 mg2+ concentrazione
■ Il Mg2+ la concentrazione è troppo alta ——Ridurre adeguatamente la concentrazione di Mg2+: ottimizzare il Mg2+ concentrazione mediante una serie di reazioni da 1 mM a 3 mM con un intervallo di 0,5 mM per determinare il Mg . ottimale2+ concentrazione per ogni stampo e primer.
A-3 Polimerasi termostabile
■ Quantità eccessiva di enzima ——Ridurre la quantità di enzima in modo appropriato a intervalli di 0,5 U.
A-4 Temperatura di ricottura
■ La temperatura di ricottura è troppo bassa ——Aumentare opportunamente la temperatura di ricottura o adottare il metodo di ricottura a due fasi
A-5 cicli PCR
■ Troppi cicli PCR ——Ridurre il numero di cicli PCR.
A-1 Primer——Scarsa specificità ——Riprogettare il primer, modificare la posizione e la lunghezza del primer per migliorarne la specificità; o eseguire la PCR nidificata.
A-2 DNA modello
——Il modello non è puro ——Purificare il modello o estrarre il DNA con i kit di purificazione.
A-3 mg2+ concentrazione
——Mg2+ la concentrazione è troppo alta ——Ridurre adeguatamente Mg2+ concentrazione: Ottimizza il Mg2+ concentrazione mediante una serie di reazioni da 1 mM a 3 mM con un intervallo di 0,5 mM per determinare il Mg . ottimale2+ concentrazione per ogni stampo e primer.
A-4 dNTP
——La concentrazione di dNTP è troppo alta ——Ridurre adeguatamente la concentrazione di dNTP
A-5 Temperatura di ricottura
——Temperatura di ricottura troppo bassa ——Aumentare opportunamente la temperatura di ricottura
A-6 Cicli
——Troppi cicli ——Ottimizza il numero di cicli

Il primo passo è scegliere la polimerasi appropriata. La normale Taq polimerasi non può correggere le bozze a causa della mancanza di attività esonucleasica 3'-5' e la mancata corrispondenza ridurrà notevolmente l'efficienza di estensione dei frammenti. Pertanto, la normale Taq polimerasi non può amplificare efficacemente i frammenti bersaglio più grandi di 5 kb. La Taq polimerasi con modifica speciale o altra polimerasi ad alta fedeltà dovrebbe essere selezionata per migliorare l'efficienza dell'estensione e soddisfare le esigenze di amplificazione di frammenti lunghi. Inoltre, l'amplificazione di frammenti lunghi richiede anche la corrispondente regolazione del disegno del primer, del tempo di denaturazione, del tempo di estensione, del pH del tampone, ecc. Di solito, i primer con 18-24 bp possono portare a una resa migliore. Per evitare danni al templato, il tempo di denaturazione a 94 °C deve essere ridotto a 30 secondi o meno per ciclo e il tempo per aumentare la temperatura a 94 °C prima dell'amplificazione deve essere inferiore a 1 minuto. Inoltre, l'impostazione della temperatura di estensione a circa 68°C e la progettazione del tempo di estensione in base alla velocità di 1 kb/min possono garantire un'efficace amplificazione di frammenti lunghi.
Il tasso di errore dell'amplificazione PCR può essere ridotto utilizzando varie DNA polimerasi ad alta fedeltà. Tra tutte le Taq DNA polimerasi trovate finora, l'enzima Pfu ha il più basso tasso di errore e la più alta fedeltà (vedi tabella allegata). Oltre alla selezione degli enzimi, i ricercatori possono ridurre ulteriormente il tasso di mutazione della PCR ottimizzando le condizioni di reazione, compresa l'ottimizzazione della composizione del tampone, la concentrazione della polimerasi termostabile e l'ottimizzazione del numero del ciclo della PCR.
Categorie di prodotti
PERCHÉ SCEGLIERE NOI
Dalla sua istituzione, la nostra fabbrica ha sviluppato prodotti di prima classe mondiale con l'adesione al principio
di qualità prima di tutto. I nostri prodotti hanno guadagnato un'eccellente reputazione nel settore e preziosa fiducia tra i clienti vecchi e nuovi.








